人教版(2019)高一化学必修二课本课后习题-----第五章
第一节硫及其化合物
1.下列物质中的硫元素不能表现出氧化性的是
A.Na2SB.SC.SO2D.H2SO4
2.下列关于SO2的叙述正确的是
A.SO2是无色、无味、有毒的气体
B.SO2与NaOH溶液反应生成
C.SO2能使紫色的溶液褪色
D.SO2有毒,不能用作食品添加剂
3.下列事实与浓硫酸表现出的性质(括号中)对应关系正确的是
A.在空气中敞口久置的浓硫酸,溶液质量增大(挥发性)
B.在加热条件下铜与浓硫酸反应(脱水性)
C.浓硫酸在白纸上书写的字迹变黑(氧化性)
D.浓硫酸可用来干燥某些气体(吸水性)
二、填空题
4.在化学课上,围绕浓硫酸的化学性质进行了如下实验探究:将适量的蔗糖放入烧杯中,加入几滴水,搅拌均匀。然后加入适量浓硫酸,迅速搅拌,放出大量的热,同时观察到蔗糖逐渐变黑,体积膨胀,并放出有刺激性气味的气体。请回答:
(1)生成的黑色物质是(填化学式)。
(2)刺激性气味的气体主要成分是(填化学式),产生该气体的化学方程式为。
(3)根据上述实验现象,表明浓硫酸具有(填序号)。
①酸性②吸水性③脱水性④强氧化性
5.如何证明酸雨中含有硫酸?请简述相关的实验操作步骤.
6.现有两支分别盛有相同体积浓硫酸和稀硫酸的试管,请用简单的方法区别它们.
7.某工厂使用的煤中硫的质量分数为0.64%,该工厂每天燃烧这种煤100 t,试计算:
(1)如果煤中的硫全部转化为SO2,该厂每天产生SO2的质量及这些SO2在标准状况下的体积;
(2)如果把产生的SO2全部用来生产硫酸,理论上每年(按365天计)可得到98%的浓硫酸的质量。
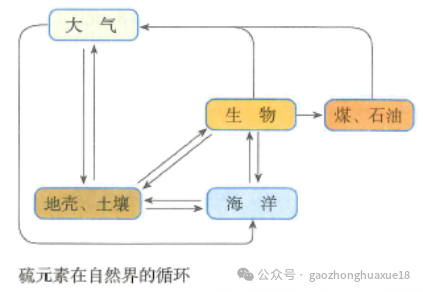
8.请分析下图,并上网查阅相关资料,简述硫在自然界的循环过程,思考人类活动对硫的循环有什么影响.
第五章第二节氮及其化合物
一、单选题
1.下列关于N2的叙述错误的是()
A.N2既可作氧化剂又可做还原剂
B.雷雨天,空气中的N2和O2可反应生成NO
C.氮的固定是将N2转化成含氮化合物
D.1molN2可与3molH2完全反应生成2molNH3
2.在NO2与水的反应中,下列说法正确的是
A.氮元素的化合价不发生变化B.NO2只是氧化剂
C.NO2只是还原剂D.NO2既是氧化剂又是还原剂
3.只用一种试剂,将Na2SO4、NH4Cl、NaCl、(NH4)2SO4四种物质的溶液区分开,这种试剂是
A.BaCl2溶液B.NaOH溶液C.AgNO3溶液D.Ba(OH)2溶液
4.根据氨气溶于水的喷泉实验,以下说法不正确的是
A.该实验证明氨气极易溶于水
B.烧瓶中充满氯气,胶头滴管和烧杯中加入浓碱液也可能形成喷泉
C.烧杯中换成其他液体无法形成喷泉
D.红色喷泉说明氨水显碱性
二、填空题
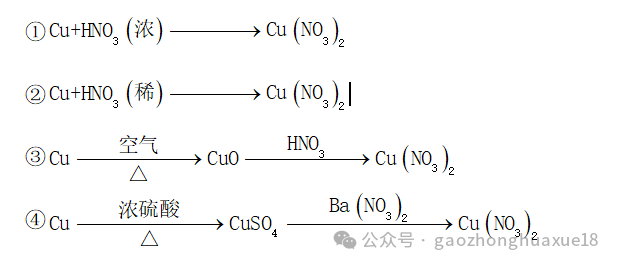
5.工业上可以废铜屑为原料制备硝酸铜,下列4种方法中,适宜采用的是哪一种?请从节约原料和环境保护的角度说明原因。
三、解答题
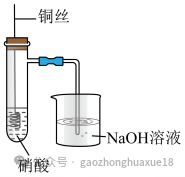
6.利用下图所示装置进行铜与硝酸反应的实验。
(1)硝酸一般盛放在棕色试剂瓶中,请用化学方程式说明其原因:。
(2)使用稀硝酸进行实验:反应开始后,铜丝逐渐变细,有气泡产生,溶液变蓝。
①铜与稀硝酸反应的离子方程式为。
②实验中观察到试管中的气体略有红棕色,其原因是(用化学方程式表示)。
(3)使用浓硝酸进行实验:反应剧烈进行,铜丝逐渐变细,溶液变绿,试管上方出现红棕色气体。
①铜与浓硝酸反应的化学方程式为。
②某同学推测反应后溶液呈绿色的原因是NO2在溶液中达到饱和,NO2的饱和溶液呈黄色,硝酸铜溶液呈蓝色,两者混合后呈绿色。他取少量该绿色溶液,向其中加入适量水后溶液变为蓝色,可能的原因是(用化学方程式表示)。
四、填空题
7.汽车尾气中含有CO、NO等多种污染物,已成为城市空气的主要污染源。汽油和柴油中基本不含氮元素,那么汽车尾气中的NO是如何产生的?请推测可能的原因,并写出有关反应的化学方程式。
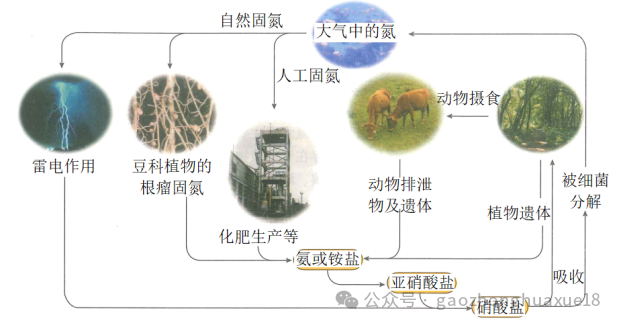
8.根据下图简单描述氮在自然界的循环过程,并思考和讨论以下问题。
(1)氮在自然界中主要以哪些形式存在?
(2)人体蛋白质中的氮是从哪里来的?
(3)自然界中有哪些固定氮的途径?
(4)人类的哪些活动参与了氮的循环?
第三节无机非金属材料
1.下列叙述错误的是()
A.硅在自然界中主要以单质形式存在B.硅是应用最广泛的半导体材料
C.高纯度的硅可用于制造计算机芯片D.二氧化硅可用于生产玻璃
2.下列物品或设施:①陶瓷餐具②砖瓦③混凝土桥墩④门窗玻璃⑤水晶镜片⑥石英钟⑦水晶项链⑧硅太阳能电池⑨光导纤维⑩计算机芯片(1)使用了硅单质的是______________(填序号,下同)。(2)使用了二氧化硅的是______________。(3)使用了硅酸盐材料的是______________
3.氢氟酸是HF的水溶液,可与SiO2发生反应生成SiF4和H2O。请写出该反应的化学方程式。想一想为什么可以用氢氟酸溶蚀玻璃生产磨砂玻璃。
4.SiO2是一种酸性氧化物,能与强碱溶液反应。例如,SiO2与NaOH反应可生成Na2SiO3。Na2SiO3的水溶液俗称水玻璃,具有黏结力强、耐高温等特性,可以用作黏合剂和防火剂。实验室盛放碱溶液的试剂瓶应使用橡胶塞,而不用玻璃塞。请解释原因,并写出相关反应的化学方程式。
5.氮化硅是一种性能优异的无机非金属材料,它的熔点高,硬度入,电绝缘性好,化学性质稳定,但生产成本较高。(1)根据以上描述,推测氮化硅可能有哪些用途:_____________(填字母)。
a.制作坩埚
b.用作建筑陶瓷
c.制作耐高温轴承
d.制作切削刀具
(2)请写出氮和硅的原子结构示意图,并根据元素周期律的知识,写出氮化硅的化学式。
(3)氮化硅在19世纪已经被化学家合成出来,但直到100多年后才逐渐应用于工业领域。材料的基础研究和实际应用之间存在着一定距离,你认为二者之间的关系是怎样的?请查阅相关资料,与同学交流你的观点。
第五章 化工生产中的重要非金属元素复习与提高
一、单选题
1.能实现下列物质间直接转化的元素是
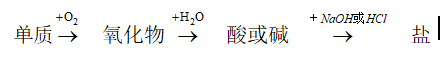
A.硫B.铁C.硅D.铜
2.下列气体中,既可以用浓硫酸干燥,又可以用固体干燥的是
A.Cl2B.O2C.SO2D.NH3
二、填空题
3.在氮的单质和常见的含氮化合物中:
(1)常用作保护气(如填充灯泡、焊接保护等)的物质是,原因是。
(2)常用作制冷剂的物质是,原因是。
(3)能与酸反应生成盐,在常温下为气态的物质是;它与盐酸等强酸反应的离子方程式是。
(4)在通常状况下是晶体,易溶于水,可用作氮肥,遇碱会放出有刺激性气味气体的一类物质是;它们与NaOH等强碱的溶液在加热条件下反应的离子方程式是。
三、解答题
4.非金属单质A经下图所示的过程可转化为含氧酸D,已知D为强酸。请回答下列问题。
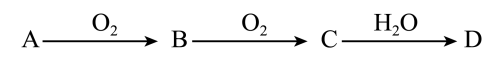
(1)若A在常温下为固体,B是能使品红溶液褪色的有刺激性气味的无色气体。
①D的化学式是。
②在工业生产中,B气体大量排放,被雨水吸收后形成的会污染环境。
(2)若A在常温下为气体,C是红棕色的气体。
①A、C的化学式分别是、。
②D的浓溶液在常温下可与铜反应并生成C气体,该反应的化学方程式为;该反应(填“属于”或“不属于”)氧化还原反应。
5.浓硫酸与木炭在加热条件下可发生化学反应,为检验反应的产物,某同学设计了如下图所示的实验。请据此回答下列问题。
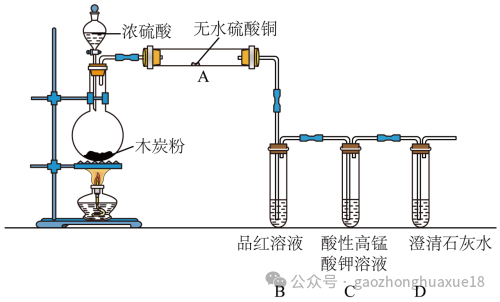
(1)A中的实验现象是。证明产物中有。
(2)B中的实验现象是,证明产物中有。
(3)装置C和D的作用是。
6.在下图所示的物质转化关系中,A是常见的气态氢化物,B是能使带火星的木条复燃的无色、无味气体,E的相对分子质量比D的大17,G是一种紫红色金属单质(反应条件和部分生成物未列出)。
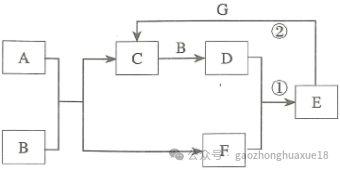
(1)A的电子式为,B的化学式为。
(2)请写出:
反应①的化学方程式
反应②的离子方程式。
四、填空题
7.氮化硅(Si3N4)可由石英与焦炭在高温的氮气流中通过以下反应制备:

(1)请写出氮化硅中氮元素的化合价,以及以上反应中的氧化剂和还原剂、。
(2)若该反应生成11.2L一氧化碳(标准状况),则生成氮化硅的质量是。
8.请用实验方法证明某无色晶体是(NH4)2SO4。
五、解答题
9.氨既是一种重要的化工产品,又是一种重要的化工原料。下图为合成氨以及氨氧化制硝酸的流程示意图。
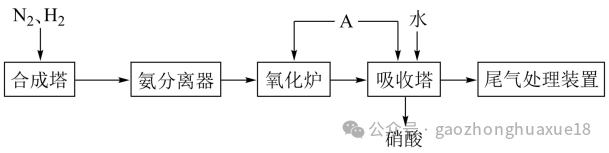
(1)写出合成塔和氧化炉中发生反应的化学方程式,并指出其中的氧化剂和还原剂。
(2)请思考A是什么物质,以及向吸收塔中通入A的作用。
(3)工业生产中为了盛装大量浓硝酸,可选择作为罐体材料。
a.铜b.铂c.铝d.镁
(4)为避免硝酸生产尾气中的氮氧化物污染环境,人们开发了溶液吸收、催化还原等尾气处理方法。前者使用具有碱性的Na2CO3溶液等吸收尾气,后者使用NH3或其他物质将氮氧化物还原为N2。请以尾气中NO2的处理为例,写出相关反应的化学方程式,并查阅资料,了解还有哪些尾气处理方法。
六、填空题
10.为测定空气中SO2的含量,某课外小组的同学将空气样品经过管道通入密闭容器中的200mL0.100mol/L的酸性KMnO4溶液。已知SO2与该溶液反应的离子方程式为:
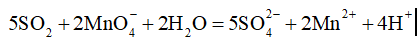
,若管道中空气流量为aL/min,经过bmin溶液恰好褪色,假定样品中的SO2可被溶液充分吸收,则该空气样品中的SO2含量(单位为g/L)是。


用户评论
这第五章感觉有点难度啊,尤其是那些有机物的结构命名和异构体问题,一直纠结好久才弄明白!希望后面章节稍微轻松点
有7位网友表示赞同!
人教版教材一向靠谱,习题难度也比较适合高中生水平。仔细做完第五章之后感觉对这章知识掌握得更扎实了!
有20位网友表示赞同!
高一化学简直是把我虐废了
本文由新途教育网发布,不代表新途教育考试网立场,转载联系作者并注明出处:https://www.contdesign.com/ptgk/546.html
相关推荐